Novavax demostró lograr una protección de cien por ciento contra la enfermedad moderada y severa
WASHINGTON, (Xinhua) — La compañía estadounidense de biotecnología, Novavax, anunció hoy que su vacuna contra la COVID-19 demostró lograr una protección de cien por ciento contra la enfermedad moderada y severa, y una eficacia general de 90,4 por ciento, en una prueba clínica de etapa avanzada.
El estudio de Fase 3 incluyó a 29.960 participantes de 119 sitios en Estados Unidos y México para evaluar su eficacia, seguridad e inmunogenicidad, con énfasis en el reclutamiento de una población representativa de las comunidades y los grupos demográficos más afectados por la enfermedad.
La vacuna, NVX-CoV2373, también reportó una eficacia de 93 por ciento contra las variantes de preocupación y las variantes de interés predominantemente en circulación, definidas por los Centros para el Control y Prevención de Enfermedades (CDC) de Estados Unidos.
Novavax
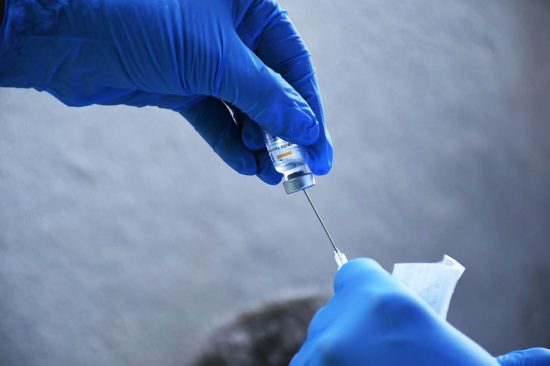
Los datos preliminares de la prueba sobre seguridad indican que la vacuna es en general bien tolerada.
Los eventos adversos graves y severos fueron pocos en número y equilibrados entre los grupos que recibieron la vacuna y los que recibieron un placebo.
«Estos datos muestran elevados y consistentes niveles de eficacia y reafirman la capacidad de la vacuna para prevenir la COVID-19 en medio de la actual evolución genética del virus», dijo Gregory Glenn, presidente de investigación y desarrollo de Novavax.
La compañía tiene la intención de solicitar autorizaciones regulatorias en el tercer trimestre de este año. En caso de ser aprobada, la vacuna de Novavax será la cuarta vacuna contra la COVID-19 autorizada para su uso de emergencia en Estados Unidos después de las vacunas de Pfizer/BioNTech, Moderna y Johnson & Johnson.





